【健康醫療網/記者黃嫊雰報導】心房顫動是引發缺血性腦中風的原因之一,據統計確診人數約為14萬至15萬人。臨床上常見使用抗凝血藥物治療,但部分患者可能面臨出血風險,醫師在決定治療選項前需謹慎評估,而過去傳統風險評估工具仍有侷限。臺大醫院總院與新竹臺大分院組成跨領域研究團隊,開發出「可解釋AI」模型,可根據個別患者的年齡、病史、用藥史等動態調整風險因子的加權比重,進行個人化評估,醫師也可掌握風險預測數值的背後原因,有助臨床實際應用的推廣。
心房顫動恐引發中風 抗凝血治療卻存在隱憂
臺大醫院內科部賴超倫主任指出,心房顫動患者多為老年族群,當心臟節律異常時,容易導致血液在左心房形成血栓,若血塊脫落後沿著血管進入腦部,便可能造成缺血性腦中風。臨床上主要透過口服抗凝血藥物降低血栓形成風險,但同時也可能增加腦或腸胃道嚴重出血的機率,使醫師必須在「使用藥物預防中風」與「避免出血風險」之間反覆權衡利弊,再做出是否用藥的決策。
現行臨床普遍使用的風險評估工具,多採用固定加權機制,將年齡、心衰竭、高血壓、糖尿病及中風病史等預測因子轉化為分數進行累加。賴超倫主任表示,該工具已使用逾二十年,不過面對複雜的個體差異時,就像西裝裁縫用硬尺測量身體各部位,臨床觀察準確度仍有限。患者若為0分,中風風險較低,可能無需使用抗凝血藥物;若為2分以上中風風險較高,建議應考慮用藥,但如果分數落於灰色地帶,則較難作為參考依據,整體預測準確表現約在6成左右。
大數據結合AI 臺大醫院打造風險評估新模型
臺大醫院研究團隊運用臺大醫院整合資料中心2007年至2016年間、約9,511名新診斷心房顫動患者資料,並利用預測模型,評估患者一年內發生缺血性腦中風的風險,研究成果已於今(2026)年4月發表於數位醫療領域權威期刊npj Digital Medicine。賴超倫主任說明,研究同時使用兩種模型進行相互驗證,一種是與傳統模型接近的「邏輯斯迴歸」模型;另一種則是「機器學習(XGBoost)」,各個預測因子的加權分數是浮動的,模型將依患者年齡、病史與用藥紀錄等因素進行動態調整。
賴超倫主任舉例,有中風病史者通常會被預測為高風險患者;而過去未曾中風者,其病史在機器學習模型中反而是保護因子。換言之,同一個因子在不同個體中,影響方向和權重也不同,與傳統模型的標準化指標呈現差異。
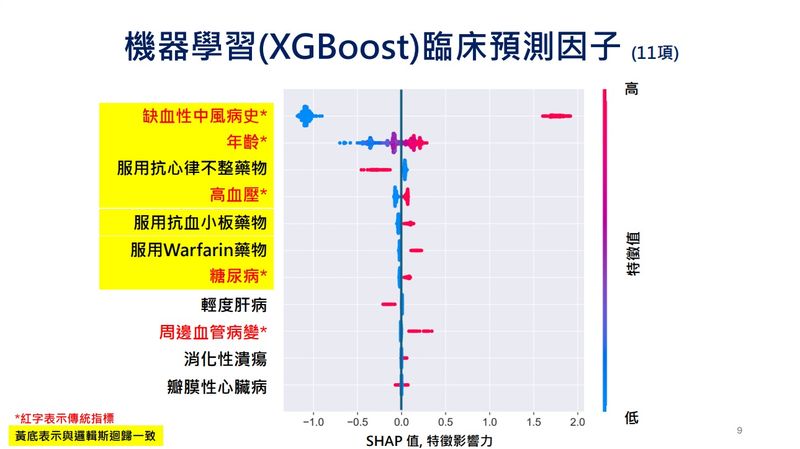
▲機器學習模型顯示不同患者的預測因子加權比重也不同。(圖/臺大醫院提供)
跨院驗證研究模型穩定性 醫師以個案說明臨床應用
為進一步驗證AI模型的穩定性與泛用性,研究團隊分別使用新竹及雲林分院共2,500筆資料進行跨院驗證,結果顯示模型預測準確度表現傾向一致。賴超倫主任分享,有一位52歲的男性罹患高血壓和心衰竭,同時服用抗心律不整藥物,在傳統指標中屬於2分以上的高風險患者,需考慮用藥;機器學習模型將其相對較輕的年齡列入考量,歸納為中度風險,經評估可能無需用藥。具體治療決策的制定,仍需綜合評估臨床指引、患者檢驗數據、影像結果等。
AI工具兼顧透明性 研究團隊:盼增加臨床信任
賴超倫主任表示,AI的應用價值在於可透過長期累積的臨床資料學習決策模式,輔助年輕醫師制定治療方案。團隊成員之一、臺大公共衛生學院流行病學與預防醫學研究所林芷瑋博士生補充,過去傳統AI醫療工具存在「黑箱」問題,其預測結果的形成機制不夠透明,包括為什麼會產生這樣的結果、每個因子扮演的角色等其實皆是未知,進而影響醫師採用意願。
林芷瑋博士生說明,本次研究所導入的「可解釋AI」概念由歐盟等機構於近年推動,旨在讓醫師可理解預測結果背後的影響因子,期待成為臨床對AI工具建立信任的起點。該模型目前則處於研究階段,在正式應用於臨床前,還需通過食藥署審查,因此未來將進行更大規模的研究,以持續驗證其效果和安全性。
【延伸閱讀】
臺大醫院啟用「電子處方箋」系統 打開手機QR Code就可至社區藥局領藥
知名韓星、羽球國手都是患者!臺大醫研究:每周一杯綠茶 鼻咽癌風險降
資料來源:健康醫療網 https://www.healthnews.com.tw/readnews.php?id=68226
喜歡本文請按讚並分享給好友!
更多健康資訊:健康醫療網https://www.healthnews.com.tw










